Antraquinonas
Disciplina de Farmacognosia I da UFPR
As antraquinonas são quimicamente definidas como substâncias fenólicas derivadas da dicetona do antraceno:
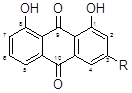
Os derivados antraquinônicos são frequentemente compostos alaranjados, algumas vezes observados in situ, como nos raios parenquimáticos do ruibarbo e cáscara-sagrada. São geralmente solúveis em água quente ou álcool diluído. Podem estar presentes nos fármacos na forma livre ou na forma de glicosídeo, isto é, na qual uma molécula de açúcar está ligada nas formas de O- e C-glicosídeo, em várias posições. O teste de Bornträger é frequentemente usado para detecção de antraquinonas livres, onde coloração rósea, vermelha ou violeta é desenvolvida em meio básico. A microssublimação também é empregada para sua caracterização, uma vez que as antraquinonas passam diretamente do estado sólido para o gasoso, cristalizando-se sob a forma de agulhas amarelas.
São empregados terapeuticamente como laxativos e catárticos, por agirem irritando o intestino grosso, aumentando a motilidade intestinal e, conseqüentemente, diminuindo a reabsorção de água.
Aula Prática
1. Caracterização microscópica de drogas com antraquinonas
- Sene: folíolos de Cassia senna L. e Cassia angustifolia Vahl, Fabaceae
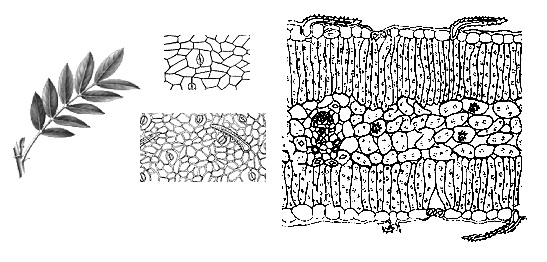

Corte transversal dos folíolos de sene. 1- tricoma tector; 2- cristal de drusa.
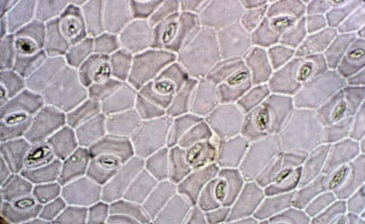
Corte paradérmico de folíolos de sene, mostrando estômatos.
- Frângula (amieiro-negro): cascas de caules de Rhamnus frangula L., Rhamnaceae

- Cáscara-Sagrada: cascas de caules de Rhamnus purshiana DC., Rhamnaceae

- Ruibarbo: rizomas (ocasionalmente raízes) de Rheum palmatum L. e Rheum officinale Baill., Polygonaceae
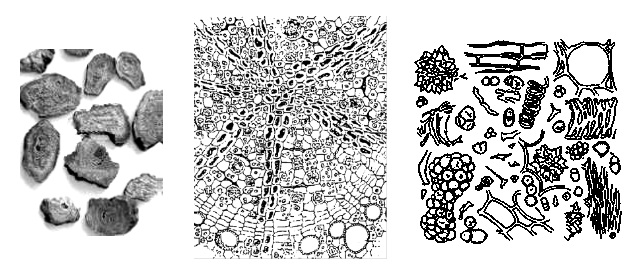
2. Identificação química de antraquinonas em plantas medicinais
-
Reação de Bornträger direta:
Para antraquinonas livres: cáscara-sagrada
- Colocar pequeno fragmento da droga (cerca de 0,2 g) ou pequena quantidade de pó em um tubo de ensaio e adicionar 5 ml de solução de NH4OH dil.
-
Reação de Bornträger com prévia hidrólise ácida:
Para glicosídeos antraquinônicos e dímeros: sene
- Colocar 1,0 g da droga em tubo de ensaio;
- Adicionar 8,0 ml de solução de EtOH a 25%;
- Ferver na chama por 1 min;
- Filtrar por algodão para um tubo de ensaio contendo 4 ml de solução H2SO4 a 5% e aquecer levemente;
- Resfriar na torneira e adicionar 5 ml de CHCl3 (clorofórmio) ou Et2O (éter etílico);
- Extrair cuidadosamente por cerca de 3 min;
- Decantar a camada orgânica para um tubo de ensaio;
- Adicionar 5 ml de solução de NH4OH dil.;
- Agitar fortemente e deixar em repouso.
3. Pesquisa de falsificação para ruibarbo
Os ruibarbos rapônicos (Rheum raponticum L.) contêm um glicosídeo, a raponticina, que apresenta atividade estrogênica, não devendo ser aplicado na medicina humana. É uma substância derivada do estilbeno (difeniletileno) com a seguinte fórmula:
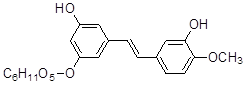
- Colocar cerca de 0,1 g de ruibarbo em tubo de ensaio;
- Adicionar 5 ml de EtOH absoluto;
- Agitar fortemente e deixar em repouso por 5 min;
- Umedecer uma tira de papel de filtro no extrato;
- Secar o papel;
- Examinar sob luz ultravioleta (ondas longas).
4. Microssublimação
- Colocar lâmina de microscopia sobre tela de amianto em suporte;
- Sobrepor anel de metal na lâmina;
- Adicionar 0,1 g da droga em pó no interior do anel;
- Colocar sobre o anel outra lâmina e aquecer;
- Trocar a lâmina superior (contendo água condensada) repetidamente até obter várias preparações (resíduo amarelo);
- Observar ao microscópio.
agulhas, que tratados com base coram-se de vermelhos (reação de
Bornträger).
Apostila de Aula Prática de Farmacognosia UEL
Objetivo: Verificar a presença ou ausência de antraquinonas ou quinonas ou antracênicos na droga vegetal.
Aula Prática
1. Reação de Bornträger direta:
- Pesar 2g da droga vegetal seca em pó e colocar em um tubo de ensaio.
- Adicionar por 2 minutos e filtrar com pouco de algodão para outro tubo de ensaio.
- Adicionar ao filtrado 1 mL da solução de NaOH a 10%. Verificar coloração rósea-vermelho.
2. Reação de Bornträger indireta com hidrólise:
- Pesar em torno de 2,0 g da droga vegetal em pó e acondicioná-la em bécker.
- Adicionar 20 mL de álcool 25% e ferver (chapa quente) durante um minuto. Filtrar em algodão.
- Transferir o filtrado para funil de separação e sobre o filtrado a quente, adicionar 30 mL de ácido sulfúrico a 5%, agitar e esfriar.
- Adicionar 20 mL de hexano e agitar vagarosamente, por inversão.
- Decantar e transferir em torno de 5 mL da camada hexânica para tubo de ensaio. Adicionar 2 a 3 mL de hidróxido de amônio diluído.
- Observar a coloração da camada amoniacal.
3. Microssublimação:
- Colocar uma pequena quantidade da droga vegetal em câmara de microssublimação e aquecer até obtenção do sublimado. Observar a coloração do sublimado.
Drogas vegetais:
Senna alexandrina (folíolos) Sinonímia científica: Cassia angustifolia Vahl, Cassia senna L. e Cassia acutifolia: Sene
Rhamnuns purshianus (casca do caule) Sinonímia científica: Frangula purshiana: Cáscara sagrada.
Rheum palmatum e R. officinale e híbridos desta espécie (rizoma): Ruibarbo.
Apostila de Aula Prática de Farmacognosia UEM
Fármacos de origem vegetal que contém heterosídeos antraquinônicos (antracênicos) são empregados desde a antiguidade como laxativos e purgativos.
Dentre as drogas mais importantes utilizadas na terapêutica, podemos citar o ruibarbo (Rheum palmatum, Polygonaceae), a cáscara sagrada (Rhamnus purshiana, Rhamnaceae), a sene (Cassia angustifolia, C. senna, Senna Alexandrina, Cesalpinaceae) e a babosa (Aloe vera, A. barbadensis e várias outras espécies, Liliaceae).
As antraquinonas são caracterizadas farmacologicamente por sua ação laxante, propriedade esta que é atribuída à presença de duas hidroxilas nas posições C-1 e C-8 e um outro grupo substituinte diferenciado em C-3. Laxantes deste tipo bloqueiam a reabsorção de sódio e água através do bloqueio da enzima ATPase dependente de Na+/K+ (efeito antirreabsortivo). Ao mesmo tempo promove, em diferentes condições, a passagem de eletrólitos e água na luz intestinal (efeito hidragogo).
Núcleo Fundamental
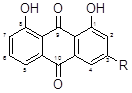
Aula Prática
Identificação das antraquinonas
1. Reação geral para identificação dos derivados antraquinônicos (Reação de Bornträger)
Empregada para detectar agliconas antraquinônicas, sendo negativa para os heterosídeos, devido a estes últimos não serem solúveis nos solventes apolares, que são o meio de reação. Pode-se eventualmente detectar as agliconas dos O- e C-heterosídeos, desde que estes sejam submetidos a uma hidrólise prévia (hidrólise ácida – H2SO4 a 20%; hidrólise oxidativa – H2O2 ou FeCl3).
Esta reação baseia-se na solubilidade dos derivados 1,8-dihidroxiantraquinônicos livres nos solventes orgânicos imiscíveis com a água (solventes apolares) e na solubilidade dos respectivos fenolatos alcalinos na água. Estes derivados quando em solução nos hidróxidos alcalinos, coram-se de vermelho ou rosa (depende da concentração dos compostos antraquinônicos na amostra analisada).
Ocorre a ionização das hidroxilas fenólicas para fenolatos hidrossolúveis.
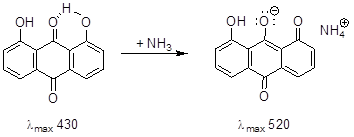
Técnica:
Ferver 300 mg da droga durante 5 minutos com 10 mL de KOH 0,5 N e 1 mL de H2O2 a 6%. Esperar esfriar e filtrar com papel de filtro. Em seguida acidificar o filtrado com ácido acético glacial (aproximadamente 10 gotas) e fazer partição com 10 mL de diclorometano. A fase orgânica deve apresentar uma coloração amarelada. A seguir separar 5 mL(*) da fase orgânica e agitar com 2,5 mL de NaOH a 2N. As antraquinonas livres conferem cor vermelha à parte alcalina e a fase orgânica torna-se incolor.
*separar os 5 mL restantes para análise cromatográfica
2. Análise cromatográfica em camada delgada:
Efetuar análise cromatográfica da parte orgânica (*) com cromatoplacas 5 x 5 cm (concentrar bem no momento da aplicação da amostra):
- fase móvel: diclorometano-metanol 83,5:16,5
- fase estacionária: sílica gel G
- revelador: placa (1) em cuba saturada com NH4OH R
placa (2) em cuba saturada com iodo
3. Pesquisa de heterosídeos antraquinônicos livres e combinados:
Antraquinonas livres
Extrair 500 mg da droga pulverizada com 5 mL de éter etílico. Deixar decantar e transferir o sobrenadante para um tubo de ensaio. Repetir o procedimento novamente e reunir os extratos etéreos. Não desprezar a droga.
Adicionar à solução etérea cerca de 1 mL de solução aquosa de NH4OH a 10% agitar. Uma coloração rósea ou vermelha na camada aquosa indica a presença de antraquinonas livres.
O-heterosídeos
Adicionar 40 mL de água destilada ao resíduo da droga obtido no item anterior e aquecer até a fervura mantendo em aquecimento brando por 10 minutos, se necessário, completar o volume com água destilada.
Esfriar e filtrar em algodão em funil para um erlenmeyer. Adicionar 5 mL de HCl concentrado e levar a ebulição, mantendo-a por 10 minutos. Esfriar e filtrar em papel de filtro para funil de separação.
Extrair a solução aquosa ácida com 3 porções (10 mL cada) de éter dietílico (não despreze a camada aquosa ácida).
Agitar 5 mL da solução etérea com 2 mL de solução NH4OH a 10%. Uma coloração avermelhada na fase alcalina aquosa indica a presença de O-heterosídeos.
C-heterosídeos
Adicionar 5 mL de solução de FeCl3 a 25% à solução aquosa ácida obtida no item anterior. Levar à ebulição branda por 15 minutos. Se necessário, adicionar mais água para completar o volume. Esperar esfriar e transferir a solução para funil de separação. Efetuar partição com 20 mL de clorofórmio. Separar a fase orgânica e lavá-la com 2 porções, de 10 mL cada, de água destilada.
Adicionar 2 mL de solução de NH4OH a 10% à 5 mL da fração clorofórmica. Uma coloração avermelhada da fase aquosa indica a presença de C-heterosídeos.
4. Microssublimação:
Neste método o calor decompõe os glicosídeos mais facilmente hidrolisáveis e como consequência as agliconas dos glicosídeos antraquinônicos são liberadas e aparecem no sublimado.
Técnica: colocar 1 g da droga em pó em um anel de vidro sobre uma lâmina e cobrir com outra lâmina de vidro, aquecer o conjunto em chapa quente até obter um sublimado amarelado na lâmina superior. Adicionar ao sublimado algumas gotas de KOH a 10% e verificar a coloração.
